Un estudio en la Universidad de Dresde en Alemania ha explorado el papel de HLA (antígeno leucocitario humano), la versión humana del complejo mayor de histocompatibilidad, en las relaciones románticas.
Estos influyen en la
selección de la pareja en los animales a través de señales
olfativas, además de ser cruciales para el correcto funcionamiento del sistema inmunológico;
es por esto que los investigadores realizaron un estudio con 580 parejas
heterosexuales en las cuales se centraron en su satisfacción en la relación,
sexual, deseo de tener hijos y percepción del olor corporal de la pareja. Los
resultados mostraron que las parejas con diferentes alelos de clase I de HLA
mostraban una mayor satisfacción general y sexual, además de encontrar el olor
corporal de su pareja mucho más atractivo y un mayor deseo de tener
descendencia con las mismas.
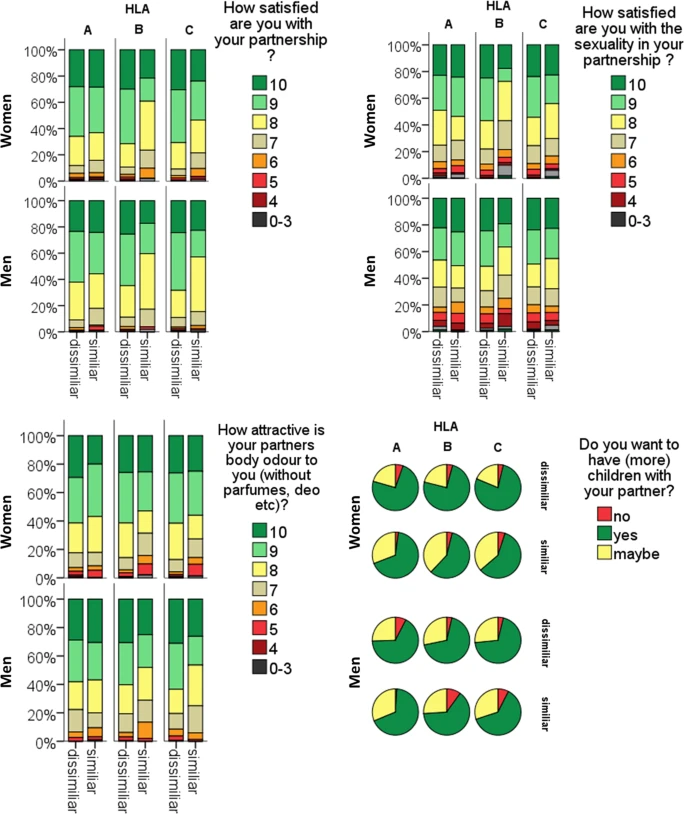 |
| El impacto de la similitud HLA en la satisfacción de la pareja y sexual, la atracción por el olor corporal y el deseo de tener hijos. |
Aun así, el estudio no
encontró gran impacto en la satisfacción de la relación o atractivo en el olor
sexual relacionado con la similitud de alelos clase II de HLA o la
heterocigosidad individual de HLA.
Esto sugiere que la diferencia particular de los alelos de clase I de HLA entre las parejas es más importante para dar forma a estas características de las relaciones humanas. El estudio apoya la teoría de que las señales olfativas mediadas por HLA influyen en la elección de pareja y en la dinámica de las relaciones humanas.
Sin embargo, los autores señalan el diseño correlacional y posibles influencias culturales, por lo que sugieren investigaciones más amplias para examinar los mecanismos subyacentes y las amplias ramificaciones, tal y como dice el artículo:
“Sin embargo, dentro del mundo de la olfacción humana, parece no
haber una pareja perfecta, sino un compañero perfecto, y esto depende de la
coincidencia de HLA”.
Imágenes: Nature
Fuente: Nature
IRL